Trial Clinici
Negli ultimi tempi numerose aziende farmaceutiche stanno sviluppando e testando dei potenziali farmaci per il trattamento della CMT; tali sperimentazioni cliniche per la CMT sono a vari livelli di avanzamento, attendiamo gli sviluppi e vi terremo aggiornati.

Quali sono le fasi per le Sperimentazioni Cliniche?
Affinché un farmaco arrivi dal laboratorio alle nostre farmacie, deve percorrere una lunga strada, fatta di numerosi controlli e studi.
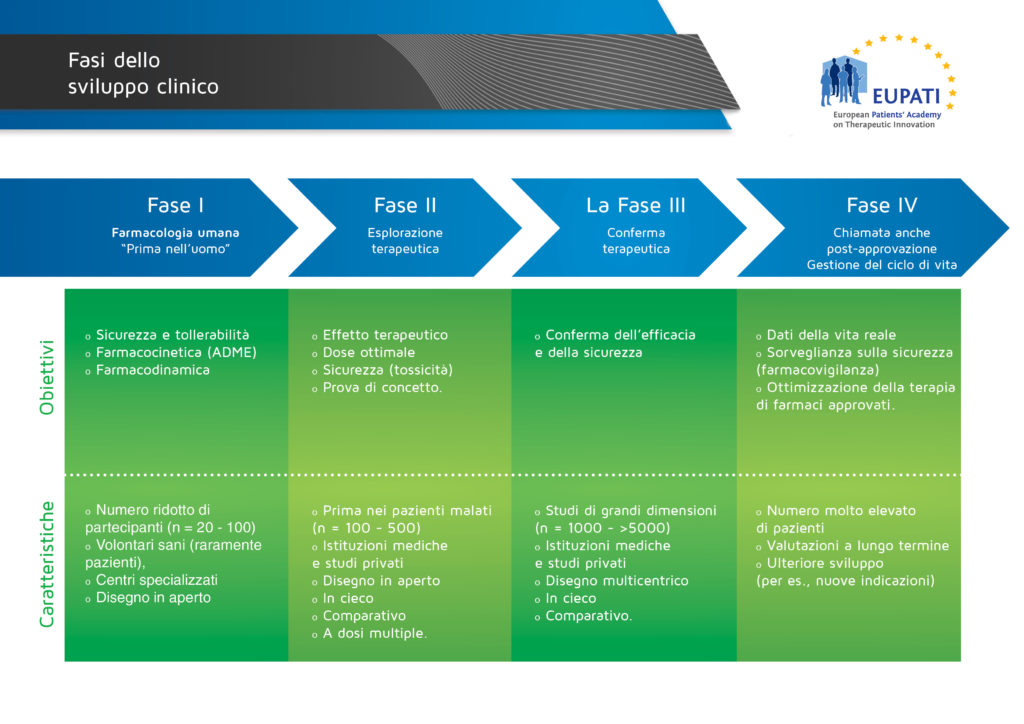
Dopo gli studi pre-clinici (sugli animali) si passa ai test sull’uomo, suddivisi in 4 fasi:
- Fase I: quanto farmaco posso dare prima che sia tossico in soggetti sani? (questa fase può essere saltata se i farmaci in questione sono già usati sull’uomo)
- Fase II: verifica del dosaggio e dell’efficacia su un numero contenuto di pazienti
- Fase III: verifica del dosaggio e dell’efficacia su un numero maggiore di pazienti
- Fase IV: Immissione in commercio e verifica di eventuali effetti non registrati nelle precedenti fasi
Elenco molecole in Sperimentazioni Cliniche per la CMT
- PXT3003: cocktail di tre farmaci, attualmente in fase III (studio di efficacia) per il trattamento della CMT1A, sviluppato da Pharnext ; come già riportato, l’FDA ha richiesto di ripetere la fase III per alcuni problemi di formulazione. A marzo 2020, l’azienda conferma l’aumento di capitale necessario per la ripetizione.
Il trial per la fase 3 “bis” per lo studio denominato “Premier” si è concluso a dicembre 2023; verrà usata una quantità doppia della dose intermedia. Inoltre, cambierà il formato che diventerà a dose singola, più facilmente gestibile. I primi risultati saranno divulgati al termine del 2023. Intanto, Pharnext ha reso noti i risultati dello studio a lungo termine.
- IFB-088: farmaco sviluppato da Inflectis Bioscience, interviene sul metabolismo delle proteine nelle cellule “stressate”. Un primo studio di fase I (studio di sicurezza/tollerabilità) ha dimostrato un buon profilo, è in corso una sperimentazione di fase II per la SLA.
- MD-1003: si tratta di una formulazione formaceutica ad alto dosaggio di biotina, una vitamina. Attualmente lo studio clinico per questa molecola è in fase I/II (valutazione della sicurezza/efficacia su un numero ridotto di pazienti) per alcune patologie demielinizzanti, tra cui la CMT
- MT-002: questa molecola sviluppata da Astrazeneca è attualmente in fase I/II (valutazione della sicurezza/efficacia su un numero ridotto di pazienti) da parte di Myotherix. Si tratta di un inibitore di un recettore (P2X7) che migliora la mielinizzazione, i livelli di calcio intracellulare e ripristina i parametri funzionali del neurone
- Neurotrophin 3 (NT-3): un approccio che sfrutta la terapia genica avente come bersaglio la CMT1A. Il vettore è in fase I/II (valutazione della sicurezza/efficacia su un numero ridotto di pazienti) per la CMT1A
- VM202 (Engensis): Helixmith ha dato il via alla sperimentazione clinica di fase I e IIa per l’utilizzo di VM202 (Engensis) per il trattamento del dolore nella CMT1A. Lo studio mira a valutare la sicurezza e la tollerabilità del farmaco; verrà somministrato nei muscoli delle gambe di dodici pazienti con CMT1A in Corea per 270 giorni. L’indice primario di efficacia confronterà la variazione dei punteggi medi giornalieri del dolore a intervalli regolari nei partecipanti trattati con Engensis rispetto al placebo. Qui i risultati della fase I.
- ACE-083: A marzo 2020, Acceleron Pharma comunica che ha deciso di interrompere lo sviluppo di questa molecola. Dallo studio di fase II (studio di sicurezza/efficacia) per il trattamento della CMT1A e 1X, è infatti emerso che, sebbene i pazienti abbiano registrato un aumento della massa muscolare dopo iniezione intramuscolare, questo non ha comportato alcun miglioramento significativo delle performance motorie
- Applied Therapeutics, un’azienda biofarmaceutica in fase clinica, sta avviando uno studio interventistico randomizzato internazionale di fase III per pazienti con deficit di sorbitolo deidrogenasi (SORD) chiamato INSPIRE. Questo studio mira a verificare la capacità del candidato farmaco AT-007 di ridurre i livelli di sorbitolo tossico rispetto al placebo e valutare l’effetto di AT-007 sul miglioramento dei sintomi della malattia per un periodo di tempo più lungo. Applied Therapeutics ha completato l’arruolamento nello studio INSPIRE di partecipanti di età compresa tra 18 e 55 anni che convivono con carenza di SORD. L’unico centro di reclutamento in Italia è l’Istituto “Carlo Besta” di Milano, coordinatore è il dott. Davide Pareyson. Leggi qui i primi risultati preliminari.
- OligoNucleotidi Antisenso, come DTX-1252, che prende di mira la malattia di Charcot-Marie-Tooth 1A (CMT1A), sono in fase di sviluppo preclinico in collaborazione con Novartis
- Inibitori della Istone Deacetilasi 6 (HDAC6), come CKD-510, sono in corso di sviluppo preclinico per il trattamento di diverse forme di CMT. A tal riguardo, Augustine Therapeutics, azienda belga che ha in sviluppo un candidato farmaco per diverse forme di CMT appartenente a questa classe ha recentemente annunciato di aver raccolto fondi per 17 milioni di euro per poter procedere alla sperimentazione clinica
- NMD670 (Ignaseclant) di NMD Pharma sta studiando un approccio innovativo e trasversale nel trattamento di diverse malattie neuromuscolari come la Charcot-Marie-Tooth: In malattie come l’atrofia muscolare spinale (SMA), la miastenia grave (MG) o la CMT ci sono problemi nella trasmissione del segnale alla giunzione neuromuscolare perché i potenziali sinaptici (la “corrente” che arriva al muscolo) sono troppo deboli. L’azienda ha recentemente ricevuto l’autorizzazione dalla Food and Drug Administration statunitense ( FDA) per la sua richiesta di avvio di uno studio clinico di fase 2, denominato SYNAPSE-CMT, del suo candidato farmaco NMD670 in pazienti affetti dalla malattia di Charcot-Marie-Tooth (CMT) di tipo 1 e di tipo 2. NMD670 è una piccola molecola inibitore del canale ionico del cloruro ClC-1 specifico del muscolo scheletrico. Sono stati pubblicati i Topline Results per il Trial 2A di Ignaseclant (NMD670).
- EnCell, Biotech Sudcoreana, ha presentato i risultati della sperimentazione di fase I su 9 persone con CMT1A, dichiarando che il loro trattamento a base di cellule staminali mesenchimali, EN001, si è rivelato sicuro senza eventi avversi gravi. Inoltre, sono stati osservati miglioramenti significativi in termini di efficacia, specie nel gruppo ad alto dosaggio. Alla luce di questi risultati, EnCell conta di ripetere il trial e verificare i benefici
- Biomarker: Numerose le sperimentazioni cliniche sui biomarcatori, parametri clinici che danno preziose indicazioni sull’andamento della malattia e l’efficacia di un trattamento. ACMT-Rete collabora attivamente a questi studi, con due sperimentazioni attive su CMT1A e CMT2A.
Scopri i trial attualmente in corso in Italia

I Lipidi come nuovi biomarcatori e potenziale bersaglio per la CMT

La Ricerca Clinica, le Sperimentazioni e le Sfide per la CMT
L’Intelligenza Artificiale al Servizio della Ricerca sulla CMT: Il Progetto Dancer

L’edizione Italiana 2025 della Guida AFM Téléthon sulla Ricerca nella CMT