Sperimentazione Preclinica per la CMT1A: Come Funziona la Nuova Terapia Genica

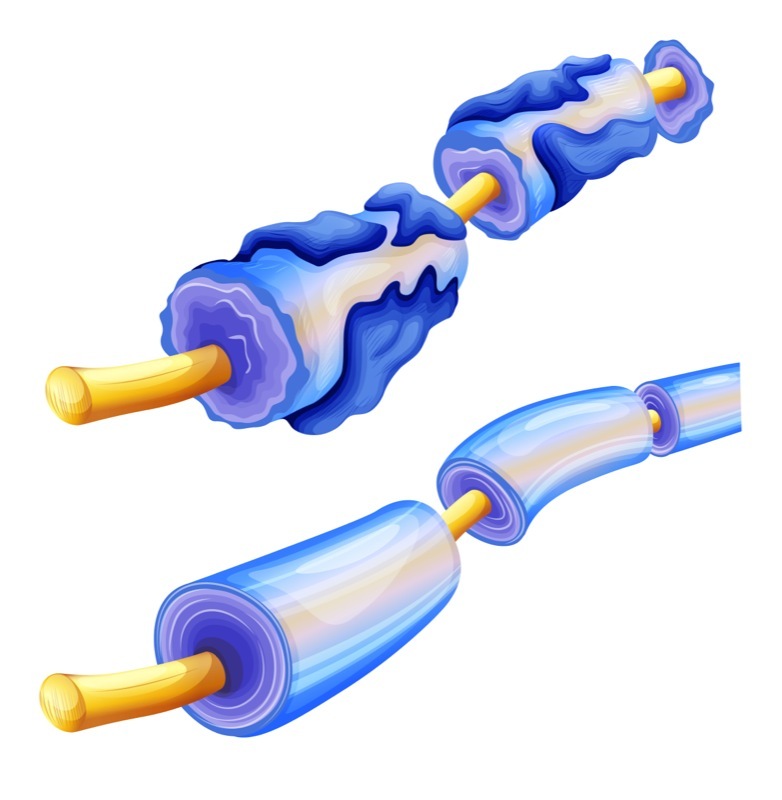
La Malattia di Charcot-Marie-Tooth di tipo 1A (CMT1A) è la neuropatia ereditaria più diffusa. È causata da un errore genetico: la duplicazione del gene PMP22. Questa duplicazione fa sì che le cellule di Schwann, responsabili della formazione del rivestimento protettivo dei nervi (la guaina mielinica), producano una quantità eccessiva e tossica di proteina PMP22. Quando questo rivestimento si danneggia, i nervi faticano a trasmettere i segnali ai muscoli, causando debolezza e perdita di sensibilità.
Un recente studio, pubblicato sulla rivista scientifica Molecular Therapy: Nucleic Acids, illustra i risultati promettenti di una nuova strategia terapeutica studiata per bloccare questa sovrapproduzione a monte, aprendo la strada verso il trattamento delle neuropatie periferiche con la terapia genica.
Il Meccanismo: Un Trasportatore e una “Forbice Molecolare”
Per curare la CMT1A, i ricercatori devono riuscire a ridurre i livelli della proteina PMP22 riportandoli alla normalità. Per farlo, hanno sviluppato un approccio in due fasi:
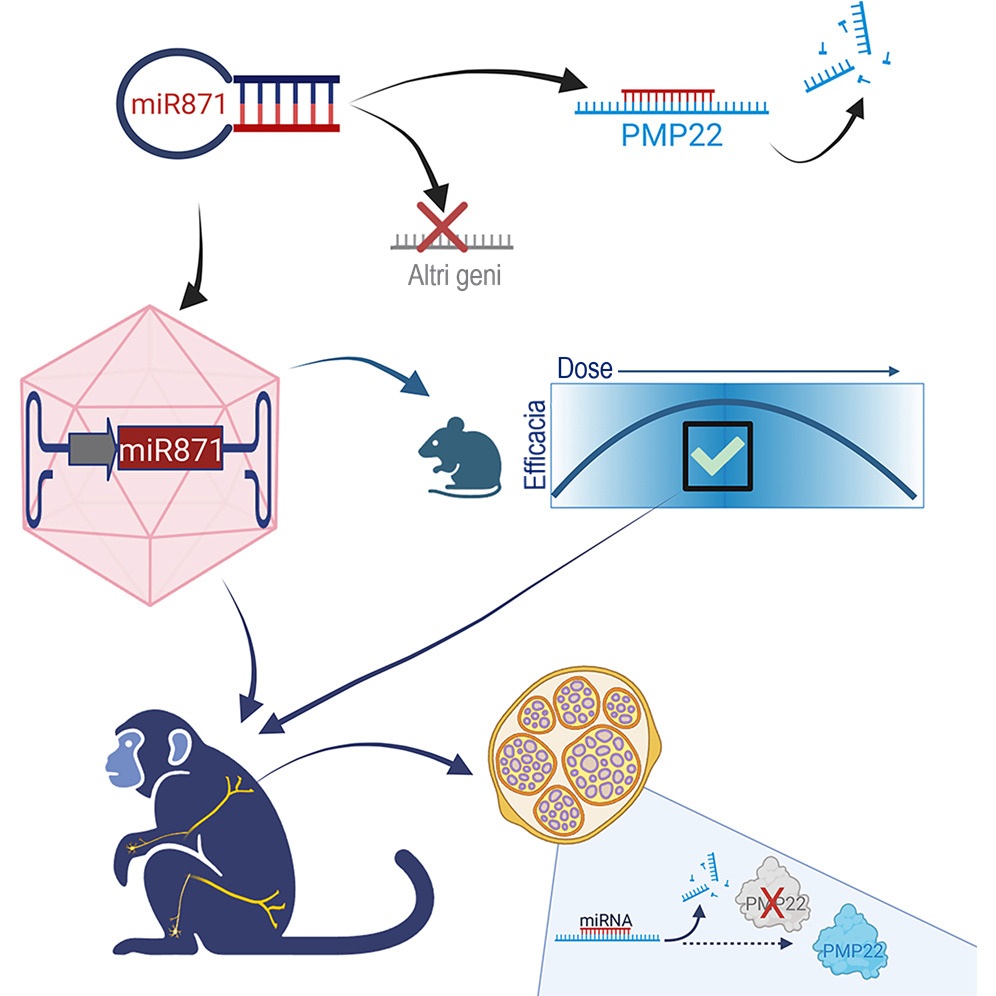
- Il veicolo di trasporto (AAV9): I ricercatori hanno utilizzato un vettore virale chiamato AAV9. Si tratta di un virus reso completamente innocuo, svuotato del suo contenuto originale e utilizzato esclusivamente come “navetta” per consegnare un messaggio terapeutico direttamente alle cellule nervose.
- La terapia (Interferenza dell’RNA): Il messaggio consegnato è una molecola (chiamata miR871) che agisce come una sorta di “forbice molecolare”. Il suo compito è intercettare e distruggere le istruzioni in eccesso inviate dal gene PMP22, prima che queste vengano trasformate nella proteina tossica.
I Risultati sui Topi: Miglioramento dei Sintomi
La terapia è stata testata su topi di laboratorio affetti da CMT1A tramite una singola iniezione lombare (nella parte bassa della schiena). I risultati sono stati molto incoraggianti:
- Riduzione della proteina tossica: Il trattamento ha ridotto con successo la quantità di PMP22 in eccesso.
- Miglioramento fisico: I topi trattati con il dosaggio ottimale hanno mostrato un netto recupero nella forza di presa e nella coordinazione motoria, tornando a livelli paragonabili a quelli dei topi sani.
- Riparazione dei nervi: Le analisi al microscopio hanno confermato che i nervi trattati presentavano una mielina più sana e spessa, segno di un rallentamento della malattia.
Il Test sui Primati: Superare la Sfida delle Distanze
Curare un topo è molto diverso dal curare un essere umano. Nell’uomo, il farmaco deve viaggiare dalla schiena fino alle estremità di nervi molto lunghi (come il nervo sciatico, che arriva fino al piede). Per verificare se il vettore AAV9 fosse in grado di coprire queste enormi distanze, la terapia è stata testata su primati non umani (scimmie).
L’esperimento ha confermato che la terapia somministrata a livello lombare è riuscita a viaggiare fino ai nervi più periferici delle braccia e delle gambe. Una volta a destinazione, ha abbassato la produzione di PMP22 fino al 53% nei nervi sciatici, dimostrando che il meccanismo funziona anche in un organismo di grandi dimensioni. Soprattutto, il trattamento si è rivelato sicuro, senza mostrare tossicità o effetti collaterali gravi per gli animali.
I Prossimi Passi
Questo studio è in fase preclinica, il che significa che il farmaco non è ancora pronto per essere somministrato ai pazienti. Tuttavia, aver dimostrato che la terapia è sicura, che riesce a viaggiare lungo i nervi distali e che riduce efficacemente la proteina tossica nei modelli animali di grandi dimensioni, rappresenta un passo essenziale. Questi dati gettano solide basi per poter richiedere l’avvio delle future sperimentazioni cliniche sull’uomo.
Fonte: “Safety, efficacy, and distal nerve Schwann cell biodistribution in mice and NHPs to support translation of AAV9 RNAi therapy for CMT1A”, Molecular Therapy Nucleic Acids, 2026.
